「社会に役立つタンパク質を自由自在に創る」
工学とは、私たちの生活を豊かにしてくれる「もの」をつくり出す学問と言ってよいかもしれません。物理学、化学、数学などの基礎研究から得られた知識を応用して工学が発展し、自動車、飛行機、高層ビル、コンピュータ、携帯電話など、我々の生活と切り離すことのできないものが数多く生み出されてきました。「タンパク質工学」も、このような工学の一種であり、タンパク質についての物理学的・生物学的な基礎研究から得られた知識を総動員して、私たちの生活を豊かにする上で役立つタンパク質を設計し創り出そうとする学問分野です。
科学的・社会的意義
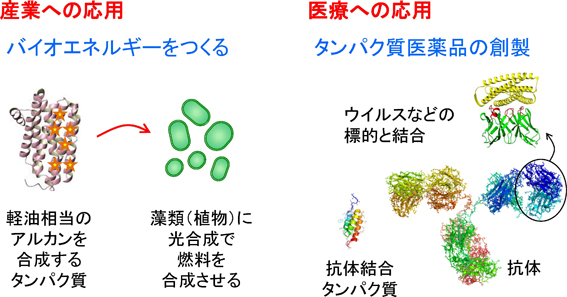
[医療への応用] タンパク質は生命現象を駆動する根源的な物質であり、人間の体内のあらゆる場所で働いているため、様々な病気と密接に関係しています。特に、抗体などのタンパク質は、ウイルスや細菌などに結合して病気を治す働きがあります(上図・右)。それゆえ、人間の健康の維持や、病気の治療に役立つ様々なタンパク質を、人工的に創り出すことができるかもしれません。タンパク質工学の分野では、これまでに10種類以上の抗体医薬品が開発され、抗がん剤等として利用されています。
[産業への応用] 微生物などの様々な生物は、医薬や工業に応用できる物質を生産したり、発酵によって食品を作ったりすることができますが、これらは全て、生物の中にあるタンパク質(酵素)の働きによるものです。したがって、タンパク質工学によって、これらの酵素のように様々な産業に利用できるタンパク質を創り出すことができるかもしれません。
[未来像] 近年、タンパク質工学の技術は目覚ましく発展してきています。医療や産業に役立つタンパク質を自由自在に設計できるようになったら、私たちの生活は一変するでしょう。このようなタンパク質工学の技術は、生命科学の時代と呼ばれる21世紀の最大の偉業の一つとして語り継がれるかもしれません。
研究概要
[目的] 医療や産業への応用がタンパク質工学の最終的な目標ですが、手法の観点から見ると、タンパク質工学の目的は主に2つに分類できます。(1) 一つは、既存のタンパク質の高性能化です。天然に存在するタンパク質の中には、例えば、石油に代わる燃料資源として利用できるアルカンを合成する酵素がありますが、その酵素活性は極めて低いため、燃料生産に利用するためには、酵素活性を向上させる必要があります(上図・左)。また、汚れを分解できる酵素を洗剤に入れて使うためには、高温や漂白剤存在下でも安定して機能を発揮できなければなりません。このように、既存の有用タンパク質の高活性化や安定化は、タンパク質工学の重要な目的の一つです。(2) もう一つの目的は、天然には存在しない新しい機能を持つタンパク質を新規に創製することです。これによって、合成の難しい物質を生物の中で生合成させたり、難治性の病気を治療したりできるようになるかもしれません。
[背景] タンパク質はアミノ酸が数珠のように連結した1本の鎖状の構造をしています。そして、アミノ酸の連結の順番(アミノ酸配列)が決まればタンパク質の立体構造が決まり、タンパク質の動き(ダイナミクス)が決まり、最終的にタンパク質の働き(機能)が決まります。また、アミノ酸の配列が変われば、タンパク質の機能が変わります。20種類のアミノ酸を100個連結させる組み合わせは20の100乗通りもあるため、アミノ酸の配列には膨大な多様性があります。特定の機能を持つタンパク質になりうるアミノ酸配列は、これらのうちの一部分です。したがって、役に立つタンパク質を設計して創り出すということは、多様なアミノ酸配列の組み合わせの中から、特定のアミノ酸配列を探し出すことに相当します。これは容易ではありませんが、主に次の2通りの方法で研究が行われています。
[方法1:合理的設計] タンパク質が機能を発揮するメカニズムを理解した上で、こういうアミノ酸配列ならばこういう機能を持つはずということを合理的に予測してタンパク質を設計する方法が合理的設計です。タンパク質の立体構造を設計するソフトウェアも開発されています。しかし現在はタンパク質のフォールディング問題が未解決のため、合理的設計の成功例は少なく、容易とは言えません。合理的設計のあと、更に下記の経験的アプローチが必要となるケースも多いです。しかし、計算機を使って有用なタンパク質を自由自在に設計できるようになったら、どんなに素晴らしいことでしょう。21世紀の間に、そのような時代がやってくると期待されています。
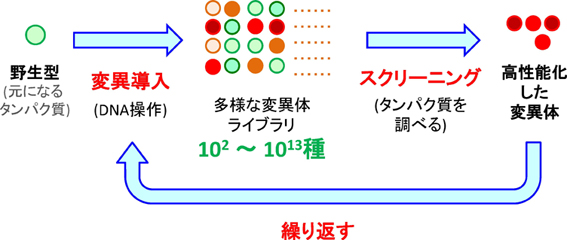
[方法2:経験的設計] アミノ酸配列の異なる多様なタンパク質分子を実際にたくさん作製し、その中から、有用なタンパク質を選別してくる方法が経験的設計です。特に、進化の原理(ランダム変異と選択)を用いて有用タンパク質をデザインする「進化分子工学」という手法が現在のタンパク質工学の主流です(下図)。ランダム変異はPCR法を応用してDNAに導入し、それらのDNAを大腸菌などに入れて多様なタンパク質(10の2~13乗通り程度)を作製します。その中から高機能性のタンパク質を選択(スクリーニング)するには、ファージ・ディスプレイ法や大腸菌のコロニーの発色などから選別する方法などが用いられます。得られた高機能性のタンパク質に再び変異を導入して更に高機能性のタンパク質を選別する、というループを何度も回すことにより、タンパク質を人工的に高速進化させることができます。このような進化分子工学的手法によって、産業用酵素や医療用抗体など、様々なタンパク質がこれまでに創り出され、実用化されています。
参考文献
新井宗仁(2013)「タンパク質の揺らぎと機能 〜結合と触媒〜」『揺らぎ・ダイナミクスと生体機能 〜物理化学的視点から見た生体分子〜』(寺嶋正秀 編)第17章 pp.267-280, 化学同人(ISBN-10: 9784759815108)
Hayashi, Y., Yasugi, F., & Arai, M. (2015) Role of cysteine residues in the structure, stability, and alkane producing activity of cyanobacterial aldehyde deformylating oxygenase. PLoS ONE 10(4), e0122217.
Kudo, H., Nawa, R., Hayashi, Y., & Arai, M. (2016) Comparison of aldehyde-producing activities of cyanobacterial acyl-(acyl carrier protein) reductases. Biotechnology for Biofuels 9, 234.
Kudo, H., Hayashi, Y., & Arai, M. (2019) Improving hydrocarbon production by engineering cyanobacterial acyl-(acyl carrier protein) reductase. Biotechnology for Biofuels 12, 291.
Kudo, H., Hayashi, Y., & Arai, M. (2019) Identification of non-conserved residues essential for improving the hydrocarbon-producing activity of cyanobacterial aldehyde-deformylating oxygenase. Biotechnology for Biofuels 12, 89.
Wada, M., Hayashi, Y., & Arai, M. (2019) Mutational analysis of a catalytically important loop containing active site and substrate-binding site in Escherichia coli phytase AppA. Biosci. Biotech. Biochem. 83(5), 860-868.
Chang, M., Shimba, K., Hayashi, Y., & Arai, M. (2020) Electrostatic interactions are essential for binding of two enzymes in cyanobacterial alkane biosynthesis. Biosci. Biotech. Biochem. 84(2), 228-237.